Columbia Üniversitesi ve ABD Enerji Bakanlığı (DOE) Brookhaven Ulusal Laboratuvarı’ndan bilim insanlarının oluşturduğu uluslararası bir işbirliği, insan hücrelerinin yüzeyinde COVID-19 virüsü SARS-CoV-2 tarafından bağlanan reseptörün büyük miktarlarda nasıl üretilebileceğini gösterdi.
Virüsün enfeksiyonunun ilk aşaması, artık meşhur olan viral spike proteini ile insan “ACE2” reseptörü arasındaki bağlanmadır.
Araştırmacılar, fare hücrelerinde insan ACE2 proteini üreterek bu reseptörleri daha iyi anlayabilir ve belki de bunlar için uygulamalar geliştirebilirler. Ayrıca bu teknik, Virology dergisinde yeni yayımlanan bir makalede ayrıntılı olarak açıklandığı üzere, geleneksel yöntemlerle üretilmesi zor olan diğer karmaşık proteinlerin araştırılmasını da kolaylaştırabilir.
Salgının başlarında Brookhaven’daki bilim insanları büyük miktarlarda insan ACE2’si üretmek ve ardından proteini nanopartiküllere bağlamak için yola çıktı. Daha sonra, ACE2 kaplı nanopartiküller antiviral ilaçlar veya virüs partikül dedektörleri olarak araştırılabilir.
Brookhaven Laboratuvarı’nın Fonksiyonel Nanomalzemeler Merkezi’nden (CFN) bilim insanları, araştırmayı yönetmek için virolog Paul Freimuth ile işbirliği yaptı. Freimuth, “Bu uygulamalardan herhangi biri için büyük miktarlarda proteine ihtiyacınız var ve proteinin tamamen işlevsel olması gerekiyor” dedi. Ancak proteinlerin hücre zarına yerleştirilme yöntemi çok karmaşık olduğundan, ACE2 gibi işleyen zar proteinleri oluşturmak çok zordur.
Salgının başlarında, Brookhaven’daki bilim insanları büyük miktarlarda insan ACE2’si üretmek ve ardından proteini nanopartiküllere bağlamak için yola çıktı. Daha sonra, ACE2 kaplı nanopartiküller antiviral ilaçlar veya virüs partikül dedektörleri olarak araştırılabilir.
Brookhaven Laboratuvarı’nın Fonksiyonel Nanomalzemeler Merkezi’nden (CFN) bilim insanları, araştırmayı yönetmek için virolog Paul Freimuth ile işbirliği yaptı. Freimuth, “Bu uygulamalardan herhangi biri için büyük miktarlarda proteine ihtiyacınız var ve proteinin tamamen işlevsel olması gerekiyor” dedi. Ancak proteinlerin hücre zarına yerleştirilme şekli çok karmaşık olduğundan, ACE2 gibi işlev gören zar proteinleri oluşturmak çok zordur.
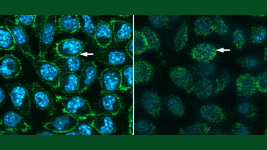
Fare hücrelerinin “yabancı” genleri ifade etme konusunda oldukça yetkin olduğu iyi bilinmektedir. Ayrıca, fare hücreleri benzer şekilde ACE2 reseptörünü üretebilse de, fare proteini SARS-CoV-2 sivri uçlarına bağlanamamaktadır. Böylece, sivri uçların hücrelere bağlanıp bağlanmadığını gözlemleyerek, bilim insanları fare hücrelerinin insan ACE2 proteinini üretip üretmediğini belirlemek için basit bir yönteme sahip olacaklardı.
ACE2 Geninin Bulunması ve Tanımı
Grup, fare hücrelerinin insan ACE2 genini emme ve doğru okuma olasılığını artırmak için bozulmamış geni kullandı. Bir proteini oluşturan amino asit yapı taşlarını kodlayan DNA dizisine ek olarak, insanlardan ve diğer “yüksek organizmalardan” gelen genler çok sayıda başka bilgi taşır. Ek veriler, hücrenin kromozomları içindeki genlerin düzenlenmesini ve çalışmasını kontrol etmeye yardımcı olur.
Sağlam ACE2 geni, içerdiği düzenleyici bilgilerle birlikte, bilim insanlarının, bizi insan yapan tüm genlerin yerlerini belirlemek için DOE destekli bir çaba olan İnsan Genom Projesi kapsamında oluşturulan klonlanmış DNA parçalarının kütüphanelerinden aldıkları bir parçada bulundu. Daha sonra fare hücrelerini, hem ölümcül bir antibiyotiğe direnç sağlayan başka bir proteinin geniyle hem de bu DNA parçasıyla kaplı nanopartiküllere maruz bıraktılar.
Freimuth’a göre bu durumda nanopartiküller, DNA’nın fare hücrelerinin kromozomlarına entegre olmasını sağlamak amacıyla hücreler tarafından emilen DNA’yı iletmek için bir araç görevi görüyor. “Yabancı geni ya da genleri alan hücreleri tespit etmek için hücre kültürlerine antibiyotik veriyoruz.
Koloniler halinde gelişen hücreler antibiyotik direnci kazanan hücrelerdi; antibiyotik direnci genini ifade etmeyen hücreler ise yok oldu.”
Bu kolonilerden yaklaşık 50 tanesi bilim insanları tarafından ayrı ayrı kültürlere bölündü ve daha sonra kaç tanesinin insan ACE2 genini de içerdiğini ve insan reseptör proteinini ürettiğini bulmak için testler yapıldı.
Proteinlerin sentezini bulmak
Freimuth’a göre insan ACE2 proteini, antibiyotiğe dirençli kolonilerin yaklaşık %70’inde hücre yüzeyinde ifade edildi. Ek araştırmaya göre, insan ACE2 geni bu kolonilerde ortalama 28 kopya halinde bulundu.
Daha da önemlisi, fare hücreleri “yabancı” ACE2 geninin kopyalarını tuttuktan sonra en az 90 hücre nesli boyunca bu genlerin kodladığı insan ACE2 proteinini üretmeye devam etti.
Fare genomuna dahil edilen ACE2 gen kopyalarının sayısı genellikle hücreler tarafından üretilen insan ACE2 proteini miktarıyla ilişkiliydi. Bazı fare hücre klonları tarafından normal fare hücrelerine kıyasla yaklaşık 50 kat daha fazla ACE2 üretildi.
Farelerde üretilen insan ACE2 proteinlerinin işlevsel olup olmadığını belirlemek için araştırmacılar bir dizi teknik kullandı. SARS-CoV-2’nin patojenik olmayan bir ikamesi olan COVID spike proteinini taşıyan bir “psödovirüsün” reseptörlere bağlanma ve hücreleri enfekte etme yeteneği bunlardan biriydi.
Freimuth’a göre bu enfektivite testleri, bu fare hücrelerinde üretilen insan ACE2 proteininin tam işlevselliğini gösterdi.
CFN’den makalenin ortak yazarları Oleg Gang ve Feiyue Teng, COVID-19’u potansiyel olarak tedavi etmek amacıyla insan ACE2 taklidi ile geliştirilmiş hücre dışı nanoveziküller üretmek için farklı yaklaşımları araştırdılar. Ayrıca, hızlı virüs tespiti veya enfeksiyon tedavisi için nanopartiküller üzerinde ACE2 proteinlerini kullanma olasılığını araştırıyorlar.
“ACE2 tabanlı nano-vesiküller SARS-CoV-2’yi nötralize etme yeteneklerini güçlendirmede bir zorluk teşkil ediyor. Virüs teşhisi için ACE2-bağlı nanopartiküllerin bağlanma hassasiyetini ve özgüllüğünü iyileştirmek ve kullanmak için de stratejiler araştırıyoruz. Çalışmanın biyolojik bileşenleri ve nanobilimdeki uygulamaları üzerinde yakından çalışan CFN araştırma görevlisi Teng’e göre, her iki strateji için de gelecekteki optimizasyon çalışmaları gerekli olacaktır.
Columbia Üniversitesi’nde ortak bir görevi olan Gang, yeni tedavi ve algılama yaklaşımları sağlamak için nanomalzemelerin üretimindeki gelişmeleri biyomoleküler tekniklerle birleştirmekten heyecan duyduğunu ifade etti. Nanomalzemeler ve biyosistemler çok çeşitli karakterizasyon teknikleri gerektirdiğinden, çalışmamız çeşitli metodolojik sorunların üstesinden gelmemize yardımcı oldu. Nanoparçacık tabanlı biyoalgılamayı geliştirmeye yönelik bir sonraki adımlarımızda burada öğrendiklerimizden faydalanacağız.”
Bu çalışma sadece çok çeşitli karmaşık proteinlerin üretilmesi için yeni bir teknik sunmakla kalmıyor, aynı zamanda rekombinant ACE2 proteini için potansiyel uygulamaların da önünü açıyor. Örnekler arasında, çeşitli biyolojik ve patolojik süreçlere aracılık eden çok çeşitli hücre yüzeyi reseptörlerinin yanı sıra enzimler ve monoklonal antikorlar gibi önemli endüstriyel uygulamalara sahip proteinler de yer alıyor.
Freimuth’a göre, bu ve diğer kritik proteinlerin büyük ölçekli sentezi, bakteri yetiştirmek için kullanılan sıvı et suyu kültürlerine benzer şekilde, muazzam süspansiyon kültürlerinde büyümek üzere değiştirilebilen fare hücreleri ile sağlam genleri birleştiren yaklaşımımızla ilerletilebilir.
Kaynak: https://phys.org/news