Yapısal biyoloji temel bir zorlukla karşı karşıyadır. Proteinler gibi biyomoleküller, karmaşık ve sürekli değişen ortamlarda dinamik olarak işlev görürler, ancak yapılarını incelemek için kullanılan başlıca yöntemler, örneğin X-ışını kristalografisi ve kriyoelektron mikroskobu (kriyoEM), kristalleştirilmiş veya dondurulmuş statik numuneler gerektirir.
Bu ayrım sadece kavramsal değil, aynı zamanda pratiktir. X-ışını kristalografisi ve cryoEM, biyokimyasal fonksiyonları incelemek için kullanılanlardan farklı, benzersiz araçlar ve uzmanlık gerektirir. Sonuç olarak, yapısal çalışmalar genellikle bu moleküllerin ilk olarak incelendiği biyoloji ve kimya laboratuvarlarından ayrı, özel laboratuvarlarda yürütülür.
Oxford Üniversitesi’nden Madhavi Krishnan ve ekibi bu boşluğu doldurmak için çalışıyor. Basit bir fiziksel soruyu yanıtlayarak biyomoleküller hakkında yapısal bilgi toplamak için bir yöntem geliştirdiler:
Bir molekülün açık silindirik bir cepten yayılması ne kadar sürer?
Bu yeni yaklaşım, X-ışını kristalografisi veya cryoEM’nin yerini almaz, ancak sürekli değişim içinde olsa bile benzer molekülleri veya aynı molekülün çeşitli konformasyonlarını ayırt etmek için yeterli veri sağlar.
Önemli bir avantajı, özel ekipman gerektirmeden biyomoleküllerin doğal çözelti fazında çalışması ve ölçümleri sadece bir dakika içinde tamamlamasıdır.
Elektrik Yüklerini Kullanarak Nanoparçacıkları Yakalama
Bu tekniğin kökeni, 2010 yılında ETH Zürich’te çalışan Krishnan’ın, elektrik yüklerini kullanarak nanoparçacıkları yakalamayı araştırmasına kadar uzanır. Nanoparçacıkları yakalamak için optik cımbızlar zaten mevcuttu, ancak bu yeni yaklaşım, negatif yüklü herhangi bir parçacığı yakalayabilirdi.
Prensip basittir: nanoakışkan bir kanalda, negatif yüklü yüzeyler itici bir elektrostatik kuvvet oluşturur ve her cebin merkezinde bir potansiyel enerji kuyusu oluşturur. Moleküller bu kuyulara yayılır ve saatlerce yakalanır.
Başlangıçta odak noktası nanopartiküllerdi, ancak bu yöntem biyomoleküller için de uyarlanabilirdi, ancak başlangıçta şüpheyle karşılandı. Krishnan, moleküllerin kaçmak için ne kadar süreye ihtiyaç duyduklarına bağlı olarak, kaçılamayan tuzaklar tasarlayarak yararlı verileri ölçebileceklerini fark etti.
Kaçma olasılığı, tuzağın enerji derinliği ve molekülün yükü ile ilgilidir. Kaçma sürelerini ölçmek, yükün kesin olarak tahmin edilmesini sağlar. Bu, molekülleri floresan etiketleyerek ve mikroskop altında gözlemleyerek yapılır. Cep dolu olduğunda parlar, boş olduğunda ise sönükleşir.
Yaklaşık on yıl boyunca, bu yük odaklı teknik geliştirildi, ancak bunun ötesinde bir potansiyel sunuyordu: yapısal verilere doğrudan erişim.
Hacimli Moleküller Kompakt Moleküllere Göre Daha Yavaş
Kaçma süresi boyuta da bağlıdır. Daha büyük moleküller, daha küçük moleküllerden daha yavaş kaçar. Başlangıçta, boyut ölçümleri, yük gibi üs değil, ön faktörde yer aldıkları için daha az hassas görünüyordu.
Boyutu vurgulamak için, molekül ve duvarlar arasındaki itmeyi azaltan tuzlar ekleyerek yükün etkisini nötralize etmek gerekir. Bu değişiklik, doktora sonrası araştırmacı Xin Zhu’nun girişimi sayesinde, yükten çok boyuta odaklanılmasını sağladı. Farklı ortamlarda kaçış sürelerini analiz ederek, bu teknik boyutla ilgili iki farklı özelliği ortaya çıkardı.
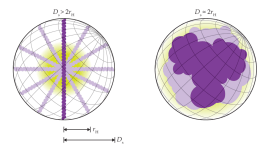
Kaçış süresi, hidrodinamik yarıçap (rH) ile doğrusal olarak ilişkilidir ve ayrıca çıkıştan geçişe (molekülü içeren en küçük küre, Ds tarafından belirlenir) bağlıdır. rH ve Ds’yi karşılaştırmak, benzer yüzey özelliklerine sahip ancak farklı iç yapılara sahip molekülleri ayırt etmeyi sağlar.
Farklı geometriler (h1 değerleri) kullanarak, iki mühendislik ürünü DNA nanoyapısı gibi, aynı yük ve kütleye sahip olanlar da dahil olmak üzere çeşitli molekül şekillerini ayırt ettiklerini gösterdiler.
Biyomoleküllerin Yapısını Hızla ve Kolayca Keşfetme
Bu teknik, farklı şekiller alan proteinler gibi formlar arasında geçiş yapan molekülleri tanımlayabilir. Algılama için floresan etiketler gerektirmesine rağmen, ışık saçılımı yoluyla etiketsiz çalışma imkanı sunan gelecekteki gelişmeler için potansiyel bulunmaktadır.
Sonuç olarak, Krishnan yeni tekniklerin öngörülemeyen olasılıklarına dikkat çekmekte ve mevcut uygulamalar konformasyon ve etkileşimleri araştırırken, beklenmedik keşifler de ortaya çıkarak anlayışı daha da genişletebilir.
Kaynaklar:
- pubs.aip.org/physicstoday/online/44377/A-quick-and-easy-probe-of-biomolecular-structure.
- X. Zhu et al., Science 388, eadt5827 (2025).
- M. Krishnan et al., Nature 467, 692 (2010).
- F. Ruggeri et al., Nat. Nanotechnol. 12, 488 (2017).
- M. Bespalova et al., Macromolecules 55, 6200 (2022).