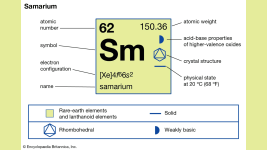
Atom numarası 62 ve sembolü Sm olan samaryum, kimyasal elementlerden biridir. Havada yavaşça oksitlenir ve biraz sert gümüşi bir görünüme sahiptir. Samaryum, lantanit grubundaki çoğu element gibi tipik olarak 3 oksidasyon durumuna sahiptir. Ayrıca samaryum(II) iyodür, samaryum(II) monoksit, samaryum(II) monokalsojenitler, samaryum(II) selenyum ve samaryum(II) Te gibi samaryum(II) bileşikleri bilinmektedir.
Fransız bilim insanı Paul-Émile Lecoq de Boisbaudran, samaryumu 1879 yılında keşfetmiştir.
Element, samarskit mineralinden sonra adlandırılmıştır. Bir Rus maden görevlisi olan Çavuş Vassili Samarsky-Bykhovets, bu minerale kendi adı verildiğinde dolaylı olarak bir kimyasal elemente adı verilen ilk kişi oldu.
Çeşitli mineraller samarskit, serit, gadolinit, monazit ve bastnäsite içerir ve son ikisi %2,8’e varan konsantrasyonlarla elementin en yaygın ticari kaynaklarıdır. Samaryum madenciliği ve üretiminde Çin ilk sırada yer almakta, onu ABD, Brezilya, Hindistan, Sri Lanka ve Avustralya takip etmektedir; bu mineraller öncelikle bu ülkelerde bulunmaktadır.
Neodimyum mıknatıslar en güçlü kalıcı mıknatıslanmaya sahipken, samaryum bileşikleri 700 ° C’nin üzerindeki sıcaklıkları tolere edebilir ve yine de kalıcı manyetik özelliklerini koruyabilir. Samaryum-kobalt mıknatıslar samaryumun en yaygın ticari kullanımıdır.
Quadramet olarak da bilinen samaryum (153Sm) leksidronam ilacı, akciğer, prostat, meme ve osteosarkom dahil olmak üzere çeşitli kanser türlerinde kanser hücrelerini öldürmede etkili olan radyoizotop samaryum-153 içerir.
Samaryum-149, önemli nötron soğurma özellikleri nedeniyle nükleer reaktör kontrol çubuklarına konulan bir başka izotoptur. Reaktör tasarımı ve işletiminde incelenen kilit hususlardan biri, reaktör işletimi sırasında bir bozunma ürünü olarak oluşmasıdır. Samaryumun X-ışını lazerleri, radyoaktif tarihleme ve kimyasal reaksiyon katalizi gibi bir dizi başka uygulaması da vardır. Kimyasal sentezde kullanılan birçok indirgeyici madde arasında samaryum (II) iyodür öne çıkmaktadır.
Samaryumun biyolojik bir işlevi yoktur ve bazı tuzları hafif zehirlidir.
Samaryum Elementinin Malzeme Özellikleri
Samaryum, çinkonun yoğunluğunu ve sertliğini paylaşan nadir bir toprak elementidir. Samaryum suda çok çözünür, bu da onu elementi cevherlerinden ayırmak için ideal bir çözücü yapar. Kaynama noktası 1,794 °C’dir, bu da onu iterbiyum ve europiumdan sonra kurşun ve baryumla eşit düzeyde üçüncü en uçucu lantanit yapar.
Samaryum yeni olduğunda gümüşi bir parlaklığa sahiptir, ancak havaya maruz kaldıktan ve oksitlendikten sonra daha az parlak hale gelir. Tahmini 238 pm atom yarıçapı ile samaryum, periyodik tablodaki en büyük elementlerden biridir ve potasyum, praseodim, baryum, rubidyum ve sezyumun arkasındadır.
Samaryum ortamdayken bir α formuna veya eşkenar dörtgen bir yapıya sahiptir.
Gerçek geçiş sıcaklığı metal saflığına göre değişir, ancak yaklaşık 731 °C altıgen yakın paketlenmiş (hcp) simetriye geçer.

Metal 922 °C’ye kadar ısıtıldığında gövde merkezli kübik (bcc) faza dönüşür.
Çift altıgen yakın paketlenmiş yapı (dhcp), 300 °C’ye kadar ısıtmanın ve 40 kbar’a kadar sıkıştırmanın sonucudur.
Yaklaşık 900 kbar’da tetragonal bir fazın ortaya çıkmasıyla sonuçlanan bir dizi faz geçişi, yüzlerce veya binlerce kilobar mertebesindeki basınçlarla indüklenir.
Bu samaryum fazının geçici doğasını doğrulayan bir çalışma, dhcp fazının, yaklaşık 400 ° C ile 700 ° C arasında hızlı bir sıcaklık değişimi ile dengesiz bir tavlama rejimi kullanılarak sıkıştırma olmadan oluşturulabileceğini bulmuştur. Samaryum buharıyla biriktirilen ince filmler normal şartlar altında hem hcp hem de dhcp fazlarını içerebilir.
Oda sıcaklığında paramanyetik özellik samaritid ve onun seskioksidi tarafından paylaşılır. Lantanitler (ve oksitleri) arasında, lutesyum ve lantanın ardından üçüncü en düşük etkin manyetik momentlere sahiptirler ve buna karşılık gelen değerler 2 bohr magnetonun altındadır. Antiferromanyetik durum, metal 14,8 K’ye soğutulduğunda elde edilir. Bunları fulleren molekülleri içine alarak, tek tek samaryum atomları ayrılabilir.
Başka bir seçenek de bunları toplu C60’ın ara boşluklarına dahil etmek ve nominal bileşimi Sm3C60 olan katı bir çözelti oluşturmaktır. Bu çözelti 8 K’de süper iletken hale gelir.
Bir tür yüksek sıcaklık süper iletkeni olan demir bazlı süper iletkenlerin normal iletkenliğe geçiş sıcaklıkları samaryum katkısı ile 56 K’ye yükseltilebilir, bu da bu seride şimdiye kadar ulaşılan en büyük değerdir.
Kaynak: Wikipedia