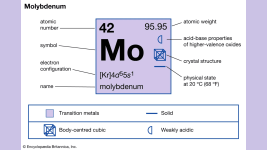
Kimyasal sembolü Mo ve atom numarası 42 olan molibden, periyodik tablonun 5. ve 6. gruplarının bir üyesidir. Cevherleri kurşun cevherleri ile karıştırıldığından, adı Neo-Latin molibdaenum’dan türetilmiştir, bu da kurşun anlamına gelen Antik Yunanca o molybdos’a dayanmaktadır. Molibden mineralleri çok uzun zamandır bilinmektedir, ancak Carl Wilhelm Scheele 1778’de elementi diğer metallerin mineral tuzlarından ayırarak ayrı bir element olarak tanımlamıştır. Peter Jacob Hjelm ilk olarak 1781 yılında metali ayırmıştır.
Molibden Dünya’da sadece minerallerdeki çeşitli oksidasyon aşamalarında serbest metal olarak doğal halinde bulunabilir. Herhangi bir elementin altıncı en yüksek erime noktasına sahip olan serbest element, gri tonlu gümüşi bir metaldir. Alaşımlarda kolayca sert, kararlı karbürlere dönüştüğü için, elementin küresel üretiminin çoğunluğu (yaklaşık %80’i) yüksek mukavemetli alaşımlar ve süper alaşımlar da dahil olmak üzere çelik alaşımlarında kullanılır.
Molibden bileşiklerinin çoğu suda az çözünürken, molibden içeren mineraller oksijen ve su ile temas ettiğinde üretilen molibdat iyonu oldukça çözünürdür. Molibden bileşikleri endüstriyel olarak yüksek basınç ve yüksek sıcaklık uygulamalarında pigment ve katalizör olarak kullanılır ve dünyadaki toplam molibden üretiminin yaklaşık %14’ünü oluşturur.
Biyolojik azot fiksasyonu sürecinde hava moleküler azotundaki kimyasal bağlantıyı koparan en yaygın bakteriyel katalizörler molibden içeren enzimlerdir. Bakteri, bitki ve hayvanlarda en az 50 molibden enzimi bulunmasına rağmen, sadece bakteri ve siyanobakterilerin azot fiksasyonu yaptığı bilinmektedir. Mo(III) ya da Mo(IV) içerdiği düşünülen demir-molibden kofaktörü FeMoco, bu nitrojenazlarda mevcuttur. Bu, bir dizi temel görevi yerine getiren diğer tüm molibden içeren enzimlerde molibdopterin ile kompleks halinde bulunan tamamen oksitlenmiş Mo(VI)’dan farklıdır. İnsanlar da dahil olmak üzere tüm yüksek ökaryotik türler, bu son enzimlerin katalize ettiği çok çeşitli kritik süreçler nedeniyle molibdene ihtiyaç duyar.
Molibdenin Fiziksel Özellikleri
Molibden, Mohs sertliği 5,5 olan ve saf halde ortalama atom ağırlığı 95,95 g/mol olan gümüşi-gri bir metaldir. Sadece tantal, osmiyum, renyum, tungsten ve karbon, doğal olarak oluşan elementler arasında 2,623 °C (4,753 °F) erime noktasından daha yüksek erime noktalarına sahiptir. Yaygın olarak kullanılan metaller arasında en düşük termal genleşme katsayılarından birine sahiptir.
Molibdenin Moleküler Bileşimi
Pauling ölçeğine göre molibden 2.16 elektronegatifliğe sahiptir ve bu da onu bir geçiş metali yapar. Oda sıcaklığında, oksijen veya su ile fiziksel olarak reaksiyona girmez. Molibden yaklaşık 300 °C’de (572 °F) zayıf bir şekilde oksitlenmeye başlar ve 600 °C’nin üzerinde toplu oksidasyon gerçekleşerek molibden trioksit üretir.
Mo3+ katyonu sıkı bir şekilde kontrol edilen koşullar altında bilinmesine rağmen, molibden birçok ağır geçiş metali gibi sulu çözeltide bir katyon oluşturma eğilimi göstermez.
Gaz halindeki diyatomik Mo2 türünden oluşur. Bu molekül bir singlettir çünkü bağlanma orbitallerinde iki eşleşmemiş elektrona ek olarak beş geleneksel bağa sahiptir. Sonuç olarak altılı bir bağ vardır.
Molibdenin İzotopları
Atom kütleleri 83 ila 117 arasında değişen dört metastabil nükleer izomer ve 35 tanınmış molibden izotopu vardır. Atom kütleleri 92, 94, 95, 96, 97, 98 ve 100 olan yedi izotop doğada bulunur. Doğal olarak oluşan bu izotoplardan sadece molibden-100 kararsızdır.
Molibdenin en yaygın izotopu olan molibden-98, tüm molibdenin %24,14’ünü oluşturur. Yarı ömrü yaklaşık 1019 yıl olan molibden-100 çift beta bozunumu ile rutenyum-100’e dönüşür. Kararsız olan tüm molibden izotopları niyobyum, teknetyum ve rutenyum izotoplarına bozunur. Oluşturulan en kararlı radyoizotop, yarı ömrü 4.000 yıl olan 93Mo’dur.
En yaygın kullanılan izotopik molibden, bir fisyon yan ürünü olan molibden-99’u kullanır. Bu, çeşitli tıbbi görüntüleme uygulamalarında kullanılan bir nükleer izomer olan teknesyum-99m’nin ana radyoizotopudur. Teknesyum-99m sadece kısa bir süre için gama ışınları yayar. Delft Teknoloji Üniversitesi 2008 yılında molibden-98 kullanılarak molibden-99 oluşturulmasıyla ilgili bir patent başvurusunda bulunmuştur.
Kaynak: Wikipedia